Nádory pankreatu jsou diagnózou léčenou v protonových centrech ve světě. Důvodem je těsná blízkost kritických orgánů a nádoru, která obvykle při použití fotonových technik neumožňuje aplikaci dostatečných dávek při současném dodržení tolerančních dávek na kritické orgány. Kromě zvýšení lokální kontroly nemoci je cílem redukce pozdních nežádoucích účinků a důraz na kvalitu života nemocných.
Nádory pankreatu mají špatnou prognózu, naproti tomu ale nevypovídají nic o tom, jak dlouho nemocný s onemocněním žije a nic o možnostech ovlivnit jeho průběh. Možnosti se rozšiřují. Navíc skupina nádorů pankreatu vůbec není homogenní. Cca 5 % nádorů pankreatu tvoří neuroendokrinní tumory „NET“, jejichž prognóza je výrazně lepší a léčebné postupy zcela jiné. Majoritní skupina epiteliálních nádorů exokrinní části pankreatu zahrnuje také méně časté formy příslušné do skupiny cystických a mucinózních nádorů pankreatu. Tyto mají také lepší prognózu a některé jsou dokonce benigní. Otázky využití léčby zářením se k NET ani k cystickým nádorům nevztahují.
Historicky má základní postavení v terapii lokalizovaných stádií ca pankreatu chirurgie – totální nebo parciální pankreatektomie. U nádorů hlavy pankreatu, které jsou nejčastější, současně duodenektomie a obnovení kontinuity anastomózami (hepatojejuno, gastrojejuno, event. pankreatojejuno nebo pankreatogastroanastomóza). Přínosná je pouze radikální resekce. Po resekcích typu R1 a R2 onemocnění časně recidivuje a vliv výkonu na délku přežívání je minimální.
Klinické studie vedené v posledních 20 letech prokázaly benefit pooperační chemoterapie a pooperační chemoterapie kombinované s ozářením (studie GITSG, EORTC a následné analýzy). Standardní léčebné postupy, které se v současné době opírají o mezinárodní konsenzus, zahrnují chirurgickou léčbu, radioterapii a chemoterapii jako neoddělitelné modality.
Srovnávací dozimetrické studie protonové vers. fotonové radioterapie lůžka pankreatu a spádových mízních oblastí prokazují jednoznačnou výhodu protonů. Redukce dávek na játra, ledviny, tenké střevo, žaludek a míchu jsou statisticky významné. U protonové radioterapie lze celkovou dávku zvýšit a dokonce aplikovat ve větších frakcích. Celková doba ozařování je pak až o 50% kratší.
Radioterapie těžkými částicemi, převážně protony, byla prakticky ověřována na několika pracovištích v USA a Japonsku. Několik dalších pracovišť se zabývalo modelováním dávkové distribuce. Publikované práce zahrnují desítky léčených nemocných. Výsledky lze shrnout:
Při pooperačním ozařování nádorů pankreatu jsou omezené a riziko nežádoucích efektů vysoké. Záměr pooperačního ozáření po resekci pankreatu je snížení rizika recidivy onemocnění. Cílový objem zahrnuje lůžko pankreatu a spádové lymfatické oblasti. Metodika určení lymfatických oblastí v riziku byla publikována. Terapeutická šíře je při pooperační radioterapii ca pankreatu minimální a to vlivem anatomického uspořádání podjaterní krajiny a složité lymfatické drenáže v oblasti.
Při využití standardních technik fotonového ozařování (3D-CRT, IMRT) je riziko nežádoucích efektů vysoké. Akutní nežádoucí efekty zahrnují zejm. gastrointestinální komplikace, akutní poradiační gastritidu a enteritidu. Časté jsou i v oblasti krvetvorby – leukopenie, trombocytopenie a po určité době i anémie. Chronické nežádoucí efekty vycházejí z poradiačního poškození jater, ledvin, event. dutých orgánů – žaludku a střeva. Statistika pozdních nežádoucích efektů není úplná s ohledem na krátké přežívání nemocných. Navíc dávky záření v referovaných souborech nepřekračují 50-56 Gy a důsledně jsou dodržovány „dose constraints“, což rizika snižuje.
Naproti tomu reference ze stereotaktické radioterapie, IMRT i 3D CRT potvrzují, eskalace dávek v cílovém objemu má potenciál zvýšení účinnosti, přirozeně také toxicity10,11). Dávky, které se v současné době aplikují v pooperační i samostatné (chemo)radioterapii, jsou submaximální a limitované poradiační toxicitou.
V PTC Praha je vyvinuta technika pooperačního ozáření lůžka pankreatu a spádových mízních cest. Ozařovaný objem je určen podle standardů RTOG. Technika aplikace svazku záření PBS (Pencil Beam Scanning) dosahuje velmi příznivé dozimetrické parametry, které jsou podkladem pro snížení toxicity.
Pooperační ozáření lze aplikovat v rozmezí 20-25 frakcí, dávka na frakci je 2,0 – 2,5 CGE. Pooperační ozáření se vždy kombinuje s chemoterapií. Ta se aplikuje ve formě tablet (capecitabin) nebo infuzí (gemcitabin) po dobu ozařování. Na pooperační ozáření navazuje standardní adjuvantní chemoterapie. Při pooperačním ozáření pankreatu je nutné dodržet důležitou zásadu – ozařování nenahrazuje pooperační chemoterapii, kterou aplikují pracoviště klinické onkologie. Obě modality jsou významné, doplňují se a zvyšují účinnost léčby. PTC Praha spolupracuje s příslušnými chirurgy i onkology tak, aby byla zajištěna návaznost všech, komplementárních, metodik.
Obrázek č. 1 Příklad ozařovacího plánu a dávkové distribuce na jednotlivé orgány – jak je z dávkové distribuce patrné, je při protonové terapii ozářeno významně menší množství zdravé tkáně.
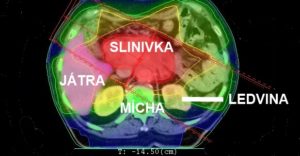
Fotonový plán
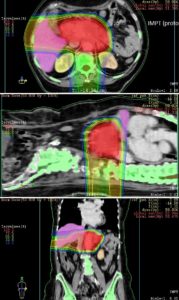
Protonový plán
Tabulka č.1 Dávka na jednotlivé strukury/orgány
| IMRT (fotony) | IMPT (protony) | |
| Cílový objem (nádor pankreasu) | 50 Gy (100%) | 50 Gy (100%) |
| Játra (Dmean) | 33 Gy (66%) | 16 Gy (32%) |
| Ledvina vpravo (Dmean) | 12.8 Gy (25.6%) | 3.4 Gy (6,8%) |
| Ledvina vlevo (Dmean) | 9.6 Gy (19.2%) | 7.5 Gy (15%) |
Kniha k zakoupení prostřednictvím odkazu níže.